Les bactéries « brassent » leur génétique pour développer une résistance aux antibiotiques à la demande
Par Célia Souque, Chercheuse postdoctorale, Microbiologie, Université d’Oxford
Pour stopper la résistance aux antibiotiques, les scientifiques ont besoin de savoir comment les bactéries deviennent résistantes.
La résistance aux antibiotiques, c’est-à-dire la capacité des bactéries novices à survivre au traitement par antibiotiques, est une menace croissante. Elle rend plus difficile le traitement d’infections potentiellement mortelles, comme la tuberculose, le SARM (Staphylococcus aureus résistant à la méthicilline) et la gonorrhée, et augmente les risques liés à des interventions chirurgicales, même mineures.
Pour résoudre le problème de la résistance aux antibiotiques, les chercheurs doivent d’abord comprendre comment empêcher la résistance de se manifester. Une étude récente que j’ai menée avec des collègues de l’université d’Oxford a permis de mieux comprendre ce phénomène en montrant que les bactéries peuvent réorganiser intelligemment leur génétique afin d’échapper aux effets d’un antibiotique.
Les bactéries ont plusieurs façons de développer une résistance. Elles peuvent muter pour empêcher les antibiotiques de les cibler, ce qui peut se faire en modifiant les protéines de la cellule où agissent les antibiotiques. Elles peuvent également acquérir des gènes qui les aident à produire des molécules destructrices d’antibiotiques, appelées enzymes.
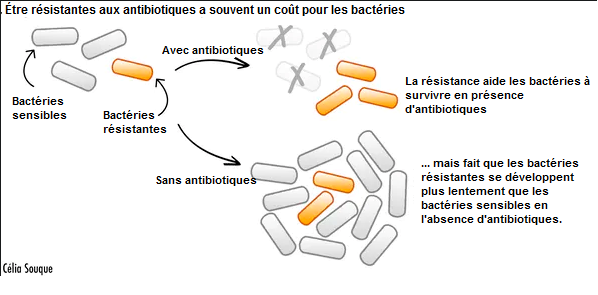
Cependant, toutes ces stratégies ont un coût pour les bactéries résistantes. La production d’enzymes de résistance nécessite beaucoup d’énergie. Les protéines modifiées ne peuvent pas non plus être aussi efficaces qu’auparavant. Ces deux facteurs entravent lourdement les bactéries et font qu’elles se reproduisent plus lentement en l’absence d’antibiotiques. Les bactéries résistantes perdent ainsi la compétition contre les autres bactéries pour les précieux nutriments et ressources, ce qui menace leur survie.
Mais les bactéries résistantes ont trouvé un moyen de devenir résistantes aux antibiotiques tout en limitant les coûts qui y sont associés. Ma récente étude a montré comment l’un de ces mécanismes, impliquant ce que l’on appelle un intégron, offre aux bactéries un potentiel incroyable pour acquérir des niveaux élevés de résistance tout en réduisant son coût énergétique. Il est donc plus facile pour les bactéries résistantes aux antibiotiques de survivre, et de prospérer.
Les intégrons sont des morceaux d’ADN, uniques aux bactéries, qui permettent à celles-ci de stocker des gènes acquis auprès d’autres bactéries résistantes. Ces gènes de résistance sont alignés l’un après l’autre dans le génome de la bactérie, formant des « réseaux ». La position des gènes dans la matrice a un impact important sur les niveaux de résistance de la bactérie.
Les gènes présents vers le début de la matrice sont fortement exprimés (ce qui signifie qu’ils sont utilisés de façon active) et offrent des niveaux de résistance élevés. Les gènes situés à l’arrière sont maintenus silencieux et peuvent être conservés à faible coût, ce qui réduit leur impact sur la bactérie.
De plus, les intégrons sont dotés d’une astuce fantastique : une enzyme, appelée intégrase, qui permet aux bactéries de couper et de déplacer les gènes dans le réseau lorsque les bactéries sont en danger. On pense que l’intégrase donne aux bactéries la capacité de « mélanger » l’ordre de leurs gènes, ce qui leur permet de moduler leur niveau de résistance à la demande. Notre étude est la première à vérifier cette hypothèse.
Pour voir dans quelle mesure les intégrons peuvent être utiles aux bactéries, nous avons construit en laboratoire des intégrons personnalisés contenant un gène de résistance pertinent en dernière position. Certains d’entre eux étaient dotés d’une enzyme intégrase présentant un dysfonctionnment, ce qui les empêchait de déplacer leurs gènes. Cela nous a permis de mesurer l’impact du brassage des gènes sur la résistance aux antibiotiques.
Nous avons ensuite utilisé une approche appelée « évolution expérimentale », dans laquelle nous avons soumis les bactéries à des doses croissantes d’antibiotiques et observé leur durée de survie. Cette technique nous a permis de mesurer directement la capacité des bactéries à développer leur résistance.
Nous avons montré que les bactéries qui pouvaient mélanger leurs gènes survivaient plus longtemps et développaient une résistance plus fréquemment que celles qui ne le pouvaient pas. Cela montre comment les intégrons peuvent aider les bactéries à développer des niveaux élevés de résistance aux antibiotiques en réponse à un traitement par antibiotiques.
Il est intéressant de noter que ce brassage est souvent lié à la perte des autres gènes de résistance présents dans la bactérie. En déplaçant les gènes pour devenir résistantes à l’antibiotique choisi, les bactéries ont perdu certains de leurs autres gènes de résistance, devenant ainsi sensibles à ces autres antibiotiques.
Nouvelles stratégies
Les résultats de notre étude fournissent des stratégies potentielles pour contrer les intégrons et leur rôle dans l’évolution de la résistance. Par exemple, les antibiotiques pourraient être associés à des médicaments capables d’inhiber l’enzyme intégrase afin de réduire le brassage des gènes. Les médicaments qui stoppent la « réponse SOS » de la bactérie – sa réaction de dernier recours aux antibiotiques – limiteraient également le brassage des intégrons. Les médicaments dits « anti-évolution », qui ne tuent pas directement les bactéries mais aident à prévenir l’évolution de la résistance, sont actuellement un domaine de recherche actif.
Une autre solution consisterait à exploiter le brassage des intégrons pour favoriser la perte des gènes de résistance en passant par différents antibiotiques. Cela permettrait d’orienter l’évolution des bactéries de manière à les rendre sensibles à des antibiotiques auparavant inutilisables.
Les intégrons sont apparus il y a des millions d’années. Mais aujourd’hui, ils se sont révélés être un mécanisme unique permettant aux bactéries de s’adapter à l’utilisation des antibiotiques par l’homme et de développer une résistance à ces derniers.
Bien que les antibiotiques sauvent d’innombrables vies chaque année, ils doivent également être utilisés avec précaution pour éviter la propagation de bactéries et de maladies résistantes aux antibiotiques. Une meilleure compréhension de la manière dont les bactéries développent une résistance nous permettra d’améliorer la manière dont nous utilisons nos antibiotiques actuels, ainsi que ceux que nous développerons à l’avenir.
Traduit par la Rédaction,, article original paru dans The Conversation UK, lien vers l’article original :
Science infuse est le média d’information en ligne de Citizen4Science, association à but non lucratif d’information et de médiation scientifique doté d’une Rédaction avec journalistes professionnels. Nous défendons farouchement notre indépendance. Nous existons grâce à vous, lecteurs. Pour nous soutenir, faites un don ponctuel ou mensuel.
