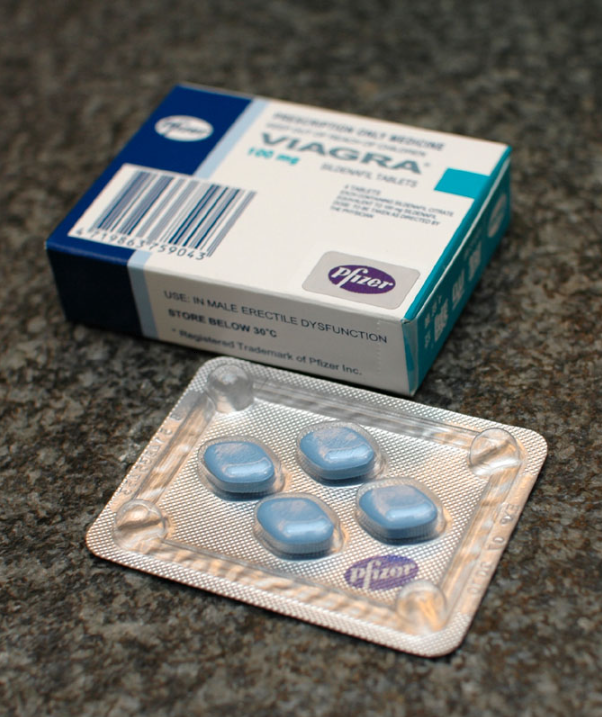
L’utilisation régulière de médicaments pour le dysfonctionnement érectile type Viagra et Cialis semble doubler le risque de problèmes ophtalmologiques graves
Une étude parue dans JAMA Ophtalmology est passée relativement inaperçue dans les médias. Elle concerne les médicaments traitant les troubles de la fonction érectile chez l’homme, comme le Viagra
Il s’agit d’une étude de cohorte rétrospective aux États-Unis publiée en ligne par JAMA le 7 avril dernier. Les chercheurs ayant mené l’étude ont en outre publié un communiqué de presse.
Sont en cause les inhibiteurs de la phosphodiestérase 5, comme les principes actifs sildénafil (Viagra de Pfizer) et tadalafil (Cialis).
Récemment, si on a beaucoup parlé du Viagra à l’occasion de la révélation de la commande de 35 000 comprimés par le Brésil pour ses soldats, la couverture médiatique de ces résultats scientifiques s’est limitée aux pays anglo-saxons et principalement les États-Unis et le Royaume-Uni.
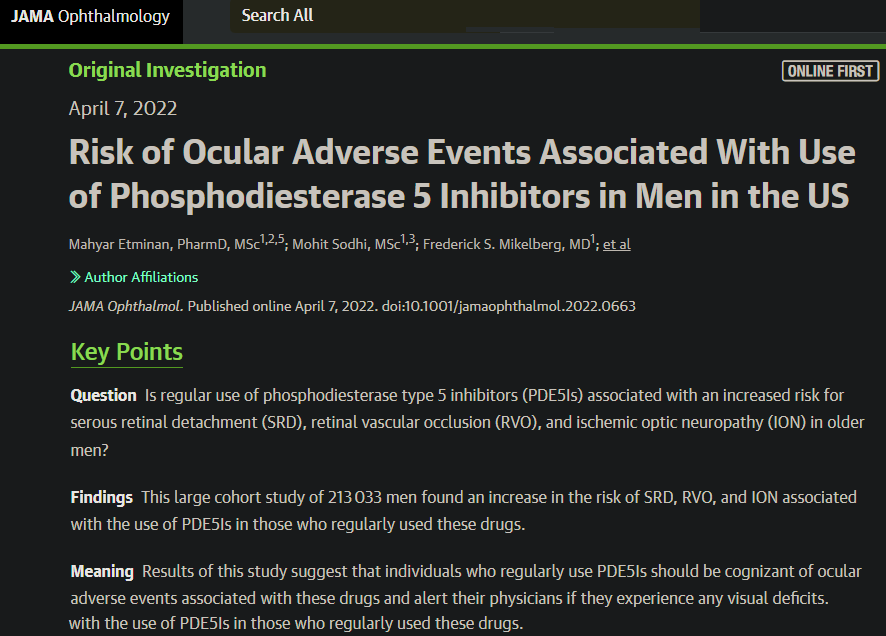
Étude observationnelle d’ampleur pour une incidence accrue de 3 affections ophtalmologiques sévères
Plus de 213 000 américains ont été inclus dans l’étude qui a révélé une incidence accrue significative des affections opthlalmologiques graves suivantes chez les utilisateurs réguliers du produit :
- décollement grave de la rétine
- occlusion vasculaire rétinienne
- neuropathie optique ischémique
Ces produits indiqués dans le dysfonctionnement érectile (DE) de l’homme ont un profil de sécurité bien établi. Par exemple, Viagra a été étudié pendant plus de deux décennies et environ 23 000 hommes ont participé aux études cliniques.
Corrélation n’est pas causalité – limitations méthodologiques
La causalité n’est néanmoins pas établie par l’étude, à ce stade, s’agissant d’une étude observationnelle avec comme caractéristique méthodologique notable néanmoins une analyse de cas-témoins emboîtés.
On peut ainsi mettre les réserves suivantes, qui font partie des faiblesses études pharmaco-épidémiologiques sur base de données secondaires saisies dans des systèmes de santé:
- les auteurs de l’étude n’ont pas eu accès aux dossiers médicaux des patients
- l’usage régulier des médicaments incriminés est supposé mais non vérifié, seules les données de prescription sont vérifiées
- En outre, vu le nombre faible d’événements indésirables recensés globalement, les données ont été regroupés pour l’ensemble des médicaments prescrits pour la classe pharmacologique, on ne peut distinguer les résultats pour chaque médicament.
Les auteurs ne sont pas ambigus à ce sujet et reconnaissent les limitations, concluant que des études supplémentaires sont nécessaires pour confirmer les résultats.
Notre question sera donc : les fabricants vont-ils prendre leurs responsabilités et prendre des mesures d’une part pour redoubler les mises en garde et surtout, faire le nécessaire pour vérifier qu’il s’agit ou non d’effets indésirables de leurs médicaments ?
Quoi qu’il en soit, cette affaire prouve que la pharmacovigilance et les études observationnelles et rétrospectives sont essentielles pour affiner le profil de sécurité d’emploi des médicaments, qui peut s’affiner tout au long du cycle de vie des médicaments.
[Expertise revendiquée de la Rédaction : expert pharmacologue, spécialiste R&D clinique]
Science infuse est un service de presse en ligne agréé (n° 0324 x 94873) piloté par Citizen4Science, association à but non lucratif d’information et de médiation scientifique doté d’une Rédaction avec journalistes professionnels. Nous défendons farouchement notre indépendance. Nous existons grâce à vous, lecteurs. Pour nous soutenir, faites un don ponctuel ou mensuel