Covid-19 : comment le coronavirus s’introduit dans notre cerveau
Entretien avec Vincent Prévot, Directeur de Recherche en Neuroendocrinologie et Neurosciences, INSERM
On sait aujourd’hui que le coronavirus SARS-CoV-2 est capable d’infecter de nombreux organes. Y compris l’un des mieux protégés d’entre eux, le cerveau. Directeur de recherche, Vincent Prévot est responsable du laboratoire Inserm “Développement et plasticité du cerveau neuroendocrine”, une composante d’un réseau de recherche européen ERC spécialisé dans l’étude du contrôle du métabolisme par le cerveau. Avec ses partenaires allemands et espagnols, ce neuroscientifique a élucidé la façon dont le virus du Covid-19 s’introduit dans cet organe sensible. Entretien mené par The Conversation
Dès le début de la pandémie, vous avez émis l’hypothèse que le coronavirus SARS-CoV-2 était capable de s’attaquer au cerveau. Comment vous est venue cette idée ?
Vincent Prévot : En 2020, comme tout le monde, nous avons été pris de court par l’arrivée de ce virus respiratoire. Nous avons alors réfléchi à la meilleure façon d’acquérir de la connaissance sur cette nouvelle maladie.
À cette époque, l’hypothèse que le virus puisse causer des dommages au cerveau n’était pas la plus en vogue, loin de là. On voyait les gens mourir d’insuffisance respiratoire ou de défaillance multiorganes, et peu de gens imaginaient que le virus était capable de passer dans le sang, donc, potentiellement, dans le liquide céphalo-rachidien, qui baigne le cerveau.
C’était d’autant moins vraisemblable que le cerveau est normalement protégé par la barrière hémato-encéphalique, une barrière physique et métabolique qui l’isole en empêchant notamment le contact direct avec le sang (ce qui limite les risques qu’un microbe qui y serait présent n’atteignent le cerveau). Pourtant, plusieurs observations nous ont amenés à considérer comme probable l’infection du cerveau par le SARS-CoV-2.
Tout d’abord, les premières données collectées indiquaient que les patients qui développaient les formes les plus graves de Covid-19 étaient majoritairement des hommes, et qu’ils étaient souvent atteints d’obésité et de diabète. Or, on sait que le cerveau contrôle en partie le dimorphisme sexuel (les différences entre hommes et femmes), notamment via l’hypothalamus. Cette structure cérébrale joue un rôle important dans de nombreux mécanismes physiologiques (régulation de la température du corps, du sommeil, de la prise de nourriture, de l’équilibre en eau, des rythmes circadiens, la reproduction…), et elle est aussi impliqué dans l’obésité et le diabète.
Il nous a donc semblé intéressant d’aller vérifier ce qui se passait à ce niveau en cas d’infection par le SARS-CoV-2. Et ce d’autant plus qu’à certains endroits de l’hypothalamus la barrière hématoencéphalique s’interrompt, pour laisser passer librement dans le sang les neurohormones produites par cette structure cérébrale. On peut donc imaginer que le virus puisse lui aussi passer par là…
Une autre structure cérébrale a également très vite attiré notre attention : le bulbe olfactif, qui traite les informations liées aux odeurs. En effet, il est apparu très tôt durant la pandémie que la perte de la capacité à percevoir les odeurs (anosmie) était un symptôme caractéristique du Covid-19. C’est parce que durant l’infection, le coronavirus SARS-CoV-2 cible l’épithélium olfactif, la muqueuse de la cavité nasale qui détecte les molécules odorantes.
Or, cet épithélium est directement connecté au bulbe olfactif, situé dans le cerveau. Là encore, nous avions une porte d’entrée possible pour le virus.
Vos partenaires allemands ont également identifié une troisième voie d’entrée, éclairant certains effets du SARS-CoV-2 sur le cerveau…
Oui. Ils ont étudié ce qui se passait chez des souris qui avaient été modifiées génétiquement pour produire, au niveau des cellules qui tapissent l’intérieur des vaisseaux sanguins cérébraux (cellules « endothéliales »), une enzyme virale indispensable au cycle de vie du SARS-CoV-2, la protéine Mpro.
Leurs travaux ont montré que Mpro s’attaque à une protéine produite par les cellules endothéliale, la protéine Nemo. Or, la destruction de Nemo désactive une voie métabolique indispensable à la survie de ces cellules. Résultat : elles meurent progressivement, ce qui endommage les vaisseaux sanguins, dont ne subsiste au final que le « squelette ».
La barrière hémato-encéphalique est ainsi rompue, et le sang, qui normalement n’accède jamais directement au cerveau, commence à fuir par ces vaisseaux « fantômes », créant des hémorragies microscopiques. Pire : une fois que les vaisseaux sont complètement morts, le sang n’y circule plus. Certaines zones du cerveau ne sont alors plus irriguées correctement.
Ce type de vaisseaux fantômes a aussi été retrouvé dans le cerveau de souris infectées par voie nasale par le coronavirus SARS-CoV-2.
Est-ce que ces résultats ont pu être vérifiés chez l’être humain ?
Oui. Nos collègues allemands ont pu avoir accès à des échantillons de cerveau provenant de malades décédés du Covid-19. En les comparant avec des échantillons de cerveau « témoins », morts d’autres causes, ils se sont aperçus que, comme chez la souris, les cerveaux des patients covidés contenaient davantage de vaisseaux fantômes que les autres.
Soulignons ici qu’accéder à ce type d’échantillon n’a pas été simple. Durant la première vague de la pandémie, les médecins, submergés par le flot des patients admis en réanimation, étaient très affectés. Dans un contexte aussi dur, il était difficile de demander aux patients qui entraient en réanimation ou à leur famille si, dans l’éventualité d’un décès, ils acceptaient une autopsie afin de faire avancer la science…
En outre, les corps des malades qui n’ont pas survécu à la maladie ont été traités très différemment selon les pays. En Italie, tous les cadavres ont été incinérés. En Allemagne, en revanche, de nombreuses autopsies ont été réalisées (plus de 300 cerveaux de personnes décédées du Covid ont pu être collectés). En France, les anatomopathologistes de notre équipe, qui travaillent dans le service de neuropathologie du CHU de Lille, ont réussi à convaincre les autorités de les laisser accéder à des cerveaux autopsiques de patients morts du Covid-19.
Nous avons de cette façon pu commencer à travailler dès juin 2020 sur les cerveaux de quatre patients décédés.
La destruction des cellules qui tapissent l’intérieur des vaisseaux sanguins cérébraux a-t-elle pu contribuer au décès des malades ? Ou entraîner des problèmes tels qu’accidents vasculaires cérébraux (AVC), voire accidents cardio-vasculaires ?
Les vaisseaux sanguins situés ailleurs que dans le cerveau ne seraient pas concernés par ce type de destruction, car la protéine Nemo, qui est attaquée par l’enzyme Mpro du virus, n’y joue pas un rôle aussi crucial que dans les vaisseaux sanguins cérébraux.
En revanche, on a effectivement observé dans le cerveau de certains patients des ruptures de vaisseaux assez sévères. On peut tout à fait imaginer que, dans les cas d’infections les plus graves, les hémorragies résultantes puissent contribuer au décès des patients, en plus des atteintes respiratoires et des autres défaillances. Des AVC ont aussi été observés.
Le cas d’un des quatre patients dont nous avons étudié le cerveau est particulièrement frappant. Le dossier médical de cette personne nous a appris que peu de temps avant de contracter le Covid-19, elle avait commencé à développer une démence vasculaire. Cette maladie liée au vieillissement évoluant très lentement, elle aurait pu vivre encore 10 ans, voire davantage.
Malheureusement, l’infection par le SARS-CoV-2 a dramatiquement accéléré les choses : une fois que ce patient a été contaminé par le coronavirus, son état s’est rapidement dégradé. Il est décédé en 6 semaines, en passant – en accéléré – par tous les stades de la démence vasculaire.
Un article scientifique décrivant ce cas clinique particulièrement singulier est en cours de publication, afin d’informer la communauté scientifique que de telles situations peuvent exister. Il faudra ensuite mener des études plus approfondies pour connaître la fréquence de ce type d’événements.
Une autre de nos découvertes suggère que la voie sanguine est importante lors de l’infection cérébrale : l’administration de mélatonine (à des doses élevées, pharmacologiques, pas aux doses habituelles de l’organisme) aux animaux, avant infection, diminue grandement la capacité du virus à gagner le cerveau, et empêche la mort des cellules endothéliales. La mélatonine est une hormone naturellement sécrétée dans le sang par la glande pinéale, qui se trouve au-dessus du cerveau.
Cette étude, menée avec nos collègues de l’Institut Cochin, suggère qu’elle pourrait exercer son effet protecteur sur les vaisseaux cérébraux, à la fois en diminuant l’expression des protéines facilitant l’infection du virus et en jouant en quelque sorte un rôle de « grain de sable » interférant avec l’arrimage du SARS-CoV2 sur la cellule dont il cible l’infection.
Nous aurions aimé étudier plus avant ce point, en utilisant notamment les cohortes de patients américains, car la mélatonine est utilisée comme complément alimentaire aux États-Unis. Malheureusement, cette molécule est prise sous des formes et des posologies très différentes d’une personne à l’autre. Pour déterminer si elle pourrait éventuellement avoir un intérêt, il faudrait monter des études plus sélectives au niveau des critères d’inclusion. Soulignons que pour l’instant, aucune preuve scientifique n’accrédite l’intérêt de la prise de mélatonine pour se protéger du Covid-19.
Les personnes qui font des formes peu sévères sont-elles aussi concernées par le risque d’atteinte cérébrale ?
Très probablement, si l’on se base sur les résultats que nous avons obtenus chez le hamster.
Il faut savoir que cet animal, qui peut, comme l’être humain, être infecté naturellement par le coronavirus SARS-CoV-2, n’est jamais victime de formes sévères. Tout au plus est-il légèrement malade pendant quelques jours, avant de guérir.
Lorsque nous avons examiné des cerveaux de hamsters covidés 20 jours après l’infection par le virus, nous n’avons pas constaté la présence de vaisseaux fantômes. Nous étions alors plutôt optimistes.
Mais lorsque, par acquit de conscience, nous avons regardé ce qui se passait au moment du pic de l’infection, quatre jours après l’entrée du virus dans l’organisme des rongeurs, nous avons eu une mauvaise surprise : les vaisseaux fantômes étaient bel et bien présents dans leur cerveau !
Ces observations constituent à la fois une bonne et une mauvaise nouvelle. La bonne, c’est que le phénomène des vaisseaux fantômes pourrait être réversible, au moins en ce qui concerne les atteintes mineures de la maladie. La mauvaise nouvelle, c’est que même dans le cas de formes peu sévères de Covid-19, ou de formes asymptomatiques, des microruptures de la barrière hémato-encéphalique (et donc des microperfusions de sang dans le cerveau) pourraient se produire.
Pendant cette courte période, ces régions du cerveau et les neurones qui y sont présents peuvent être fragilisés. Reste à vérifier ce qui se passe précisément chez l’être humain…
Quelles pourraient être les conséquences de ces ruptures microscopiques ?
Certains neurones peuvent mourir, d’autres peuvent moins bien vieillir. Cela pose la question de savoir si l’infection par le SARS-CoV-2 n’aura pas des conséquences sur le vieillissement de notre cerveau, dans 20 ou 30 ans.
Une étude anglaise publiée récemment dans la revue Nature est particulièrement frappante. Avant la pandémie, ses auteurs avaient prévu d’étudier par IRM le vieillissement du cerveau, en mobilisant une cohorte de 300 participants. Après la première IRM, la première vague de coronavirus a déferlé. Lorsque les patients ont été convoqués à nouveau pour l’IRM suivante, la moitié avait contracté le virus. Les nouvelles IRM ont alors révélé que, chez les gens qui avaient été infectés par le SARS-CoV-2, certaines structures cérébrales avaient changé de forme. En outre, les performances cognitives étaient parfois détériorées, surtout chez les participants les plus âgés.
À ce propos, nous sommes particulièrement préoccupés par ce qui pourrait se passer chez les enfants. Grâce à des travaux financés par l’ANRS et la Fondation pour la Recherche médicale, nous avons en effet pu étudier plus précisément un type particulier de neurones, les neurones à GnRH. Durant la vie fœtale, ces neurones prennent naissance dans le nez, puis migrent dans le cerveau. Ils contrôleront à l’âge adulte la fonction de reproduction.
Nous avons découvert que ces neurones à GnRH expriment fortement le récepteur ACE2, qui est utilisé par coronavirus SARS-CoV-2 comme « serrure » pour s’introduire dans les cellules. On peut donc craindre que ces neurones soient attaqués et détruits par le virus. Cela pourrait poser problème, car en temps normal, leur activation une semaine après la naissance est à l’origine d’un phénomène appelé « mini-puberté ».
Cette période du développement, qui existe chez tous les mammifères, correspond à la première activation des ovaires et des testicules, qui aboutit à la première sécrétion d’hormones stéroïdes gonadiques (œstrogènes et testostérone). Ces deux hormones exercent à leur tour une rétroaction sur le cerveau. Nous ne savons pas encore quelles sont les conséquences de cette rétroaction sur la maturation cérébrale, mais un projet européen est en cours pour le déterminer.
Il s’agira de comprendre si des enfants qui ont une mini-puberté altérée risquent de développer des maladies non communicables, telles que des troubles de l’apprentissage, des problèmes de fertilité, des maladies métaboliques comme le diabète ou l’obésité, etc.
C’est toute la difficulté à laquelle sont confrontés les scientifiques : les informations sur le Covid-19 arrivent de toutes parts. Il faut maintenant constituer des cohortes pour pouvoir extrapoler, déterminer les facteurs de risque, et tirer des conclusions à l’échelle de la population, par classes d’âge, en fonction de l’état de santé, etc. Il est important d’avoir un nombre de participants important pour ce type d’études, car nous avons par exemple remarqué que, chez les souris covidées, l’infection du cerveau n’était pas systématique.
Entretien mené et publié initialement pars The Conversation
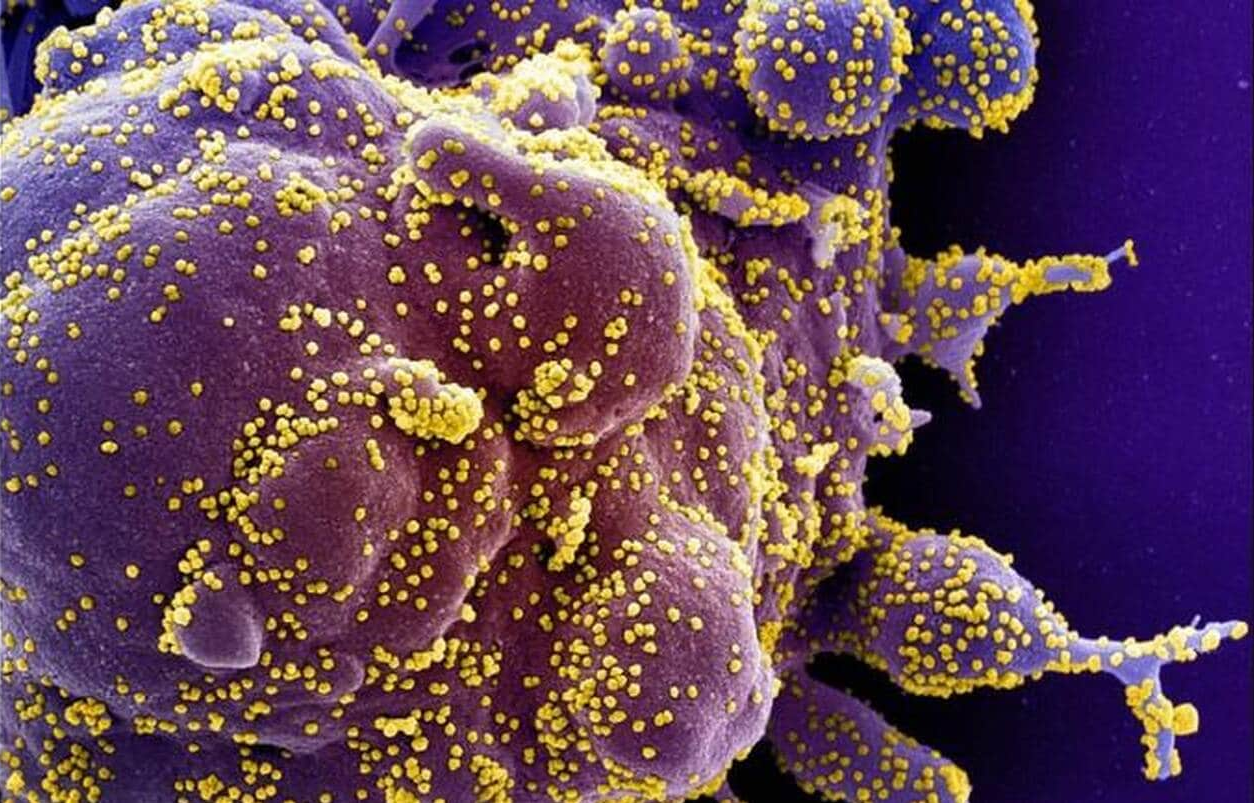
Image d’en-tête : Micrographie électronique à balayage d’une cellule apoptotique (en violet, fausses couleurs) infectée par le SARS-CoV-2 (particules jaunes, fausses couleurs), isolée à partir d’un échantillon provenant d’un patient. National Institute of Allergy and Infectious Diseases, NIH
Science infuse est un service de presse en ligne agréé (n° 0324 x 94873) piloté par Citizen4Science, association à but non lucratif d’information et de médiation scientifique doté d’une Rédaction avec journalistes professionnels. Nous défendons farouchement notre indépendance. Nous existons grâce à vous, lecteurs. Pour nous soutenir, faites un don ponctuel ou mensuel.
ou via J’aime l’Info, partenaire de la presse en ligne indépendante



Ping : Le Covid augmenterait de 50 à 80 % le risque d'apparition de la maladie d'Alzheimer dans les 12 mois chez les personnes âgées, selon une grosse étude de cohorte américaine - Citizen4Science