Maladie de Parkinson : une étude clinique évaluant le médicament antidiabétique lixisénatide donne de l’espoir pour ralentir la progression
Après le diabète de type 2 et l’obésité, les analogues du GLP-1 à l’instar du sémaglutide (Ozempic, Wegovy) sont-ils une poule aux œufs d’or multipotente ? Restons prudents, mais une étude de phase 2 menée par une équipe de recherche française fournit des résultats encourageants. Résultats et enjeux
Nous évoquons régulièrement dans ces colonnes cette nouvelle classe pharmacologique des analogues du GLP-1 (glucagon-like peptide 1) dont la première née est le sémaglutide, commercialisée dans le traitement du diabète et qui a généré l’« affaire » Ozempic, détourné comme coupe-faim. Le repositionnement de la molécule dans l’indication obésité est en cours.
Nouvelle cible thérapeutique pour la classe pharmacologique : la maladie de Parkinson, maladie dégénérative pour laquelle on manque cruellement de traitement efficace pour stopper l’évolution inexorable de la maladie. Le lixisénatide est commercialisé en Europe par le laboratoire Sanofi sous le nom de Lyxumia dans le diabète de type 2, en concurrence avec Wegovy de Novo-Nordisk entre autres.
L’étude a été publiée le 3 avril par les chercheurs, dont principalement les professeurs Olivier Rascol du CHU de Toulouse et Wassilios Meissner du CHU de Bordeaux dans la prestigieuse revue médicale New England Journal of Medicine.
Mais que justifie de tester un antidiabétique dans la maladie de Parkinson, qui affecte plus de 175 000 personnes dans notre pays et pour laquelle il n’y a pas d’innovation thérapeutique majeure depuis des décennies ?
Piste du risque accru de diabète en cas de maladie de Parkinson
Il est important de préciser qu’en recherche clinique, toute étude se doit d’être justifiée d’un point de vue éthique. Notamment, on ne teste pas un médicament expérimental chez n’importe qui, pour voir ou « au cas où ».
Pour le lixisénatide, les chercheurs avaient donc une piste : le fait que les patients atteints de diabète sont plus susceptibles de développer une maladie de Parkinson que dans la population générale. Mais ce n’est pas tout : des études sur le mécanisme du diabète laissent également penser que la maladie est associée à une perte de neurones particuliers dans le cerveau. C’est ainsi que les chercheurs ont émis l’hypothèse que des antidiabétiques comme le lixisénatide pouvaient peut-être avoir un effet neuroprotecteur pour les neurones dopaminergiques, ceux affectées par la maladie de Parkinson et qui produisent la dopamine, le neurotransmetteur qui est en déficit dans la maladie de Parkinson.
Un médicament neuroprotecteur serait une avancée thérapeutique majeure, car aujourd’hui on ne dispose que de substituts à la dopamine (les médicaments dopaminergiques), dont l’effet s’épuise au fil du temps.
« LixiPark », une étude de phase précoce au début d’un long parcours de recherche chez les malades
Une méthodologie d’étude irréprochable, des résultats cliniques robustes, des effets indésirables essentiellement gastro-intestinaux
Il s’agit d’une étude clinique réalisée dans plusieurs centres d’étude en France, de phase 2, soit de première administration chez des patients atteints de la pathologie pour laquelle on évalue le traitement expérimental. Elle est menée chez un nombre limité de patients, ici 156. D’un point de vue méthodologique, l’étude applique l »‘étalon-or » : l’étude clinique randomisée en double aveugle contre placebo. Faisons-un petit point à ce sujet, pour notre culture médico-scientifique :
Méthodologie
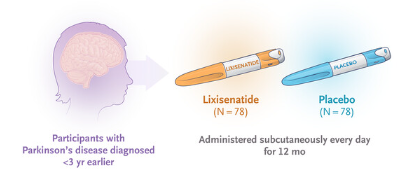
Les participants à l’étude devaient être âgés de 40 à 75 ans et atteints de maladie de Parkinson précoce, c’est-à-dire avec un diagnostic posé moins de 3 ans avant l’entrée dans l’étude. Ils devaient recevoir une dose stable de médicament dopaminergique (traitement standard de la maladie) depuis au moins un mois.
Les patients sélectionnés ont reçu une administration quotidienne du médicament de l’étude, par voie sous-cutanée, pendant 12 mois. Par médicament de l’étude, il faut comprendre soit le médicament expérimental lixisénatide, soit un placebo, produit qui ne contient aucune substance active. Ainsi les participants ont reçu pour la moitié d’entre eux le lixisénatide, l’autre moitié le placebo. Ni les chercheurs ni les patients ne savaient ce que recevait les participants (c’est ce que l’on appelle le « double-aveugle »). En outre, l’attribution de l’un ou l’autre des produits aux participants étaient le fruit du hasard, part tirage au sort avec un programme informatisé (c’est ce que l’on appelle la « randomisation »).
Résultats d’efficacité clinique
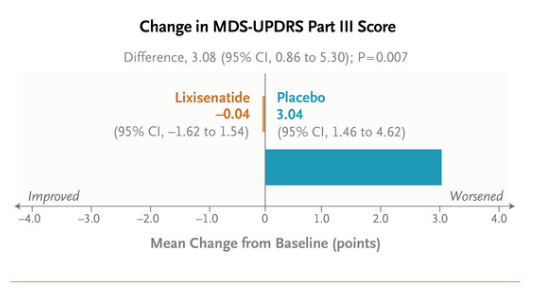
Le critère d’efficacité principal était la variation par rapport à l’entrée dans l’étude du score d’une échelle clinique de référence de l’évaluation de troubles du mouvement, qui sont les principaux signes cliniques de la maladie de Parkinson. Un échelle de mesure de score de ces mouvements validée scientifiquement et dédiée à la maladie de Parkinson a été utilisée, la partie III de l’échelle MDS-UPDRS (Movement Disorder Society-Unified Parkinsons’s Disease Rating Scale).
Plus le score est élevé, plus l’intensité des signes de mouvements anormaux associés à la maladie de Parkinson sont importants.
Quel est le résultat de l’étude ici ? Les patients n’ont quasiment pas vu d’évolution de leur score à cette échelle après 12 mois de traitement dans le groupe prenant du lixisénatide (évolution moyenne du score : -0,04). Faut-il en conclure que le médicament expérimental n’a pas d’effet ?
Surtout pas ! et c’est là que l’on voit l’intérêt du groupe placebo : ceux qui l’on pris on vu leur score à l’échelle augmenter en moyenne de 3,04 à la fin de l’étude.
Ces résultats sont statistiquement significatifs permettant de conclure que la prise du médicament expérimental a permis de freiner l’évolution naturelle des troubles du mouvement des malades parkinsoniens.
Résultats de tolérance
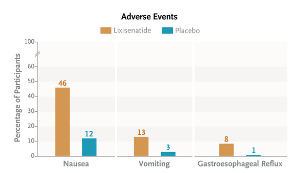
L’intérêt d’un médicament s’apprécie toujours en étudiant le rapport entre ses bénéfices et ses risques. L’étude LixiPark a donc soigneusement répertorié les éventuels événements indésirables survenus pendant l’étude. Après avoir recensé tous les événements indésirables survenus, on a constaté un nombre significativement plus importants de tels événements chez les patients ayant pris du lixisénatide, soit près de la moitié d’entre eux. Il s’agit principalement de troubles gastro-intestinaux, en premier lieu des nausées, ainsi que dans une moindre mesure des vomissements et des reflux gastro-œsophagiens. La différence de fréquence de survenue des effets est significative avec ceux survenus dans le groupe placebo, ce qui permet de penser que la molécule expérimentale est en cause dans l’augmentation de la survenue des effets en question.
Pas de conclusions hâtives mais un intérêt à poursuivre le développement
On ne tire en aucun cas de conclusions fermes ou définitives d’une étude de phase 2 menée auprès de quelques dizaines de patients ayant reçu le traitement expérimental. Ces résultats positifs de limitation de la progression de l’incapacité motrice due à la maladie de Parkinson permettent d’espérer que des études à plus grande échelle, c’est-à-dire de phase 3, pourront confirmer les bienfaits du lixisénatide. Il faut aussi noter que dans dans l’étude LixiPark, il a été donné comme traitement complémentaire à un traitement de fond par un médicament standard pour la maladie de Parkinson, et non en remplacement de ce dernier.
Le traitement expérimental a duré un an et se limite à des patients en phase précoce. LixiPark ne permet pas de savoir si le lixisénatide conserve ses effets s’il est administré plus longuement, et s’il est bénéfique à des stades ultérieurs de la maladie de Parkinson. On ne sait pas non plus quel peut être le mécanisme d’action de l’éventuel effet neuroprotecteur du lixisénatide, même si on pense à un effet réducteur de l’inflammation sur les neurones suite à des études sur la souris.
Ainsi, les résultats de cette étude, si elles ouvrent une voie de développement et de l’espoir, amènent également tout un lot de questions désormais ouvertes et auxquelles les chercheurs vont tenter de répondre avec de nouvelles études dans le futur.
Image d’en-tête : Michael J. Fox, acteur américain, atteint de la maladie de Parkinson précocement, recevant en 2008 un doctorat honoris causa de l’université de New York pour sa contribution à la recherche – Source Wikipédia
Pour aller plus loin
Science infuse est un service de presse en ligne agréé (n° 0329X94873) piloté par Citizen4Science, association à but non lucratif d’information et de médiation scientifique.
Notre média dépend entièrement de ses lecteur pour continuer à informer, analyser, avec un angle souvent différent car farouchement indépendant. Pour nous soutenir, et soutenir la presse indépendante et sa pluralité, faites un don pour que notre section presse reste d’accès gratuit, et abonnez-vous à la newsletter gratuite également !
ou via J’aime l’Info, partenaire de la presse en ligne indépendante



