L’environnement des cellules déraille aussi lors des cancers !
par Zeinab Rekad, Doctorante, Univesité Côte d’Azur
Découvrez « Will you be my valentine? », une superbe image de science de la photothèque du CNRS, commentée par son auteur !
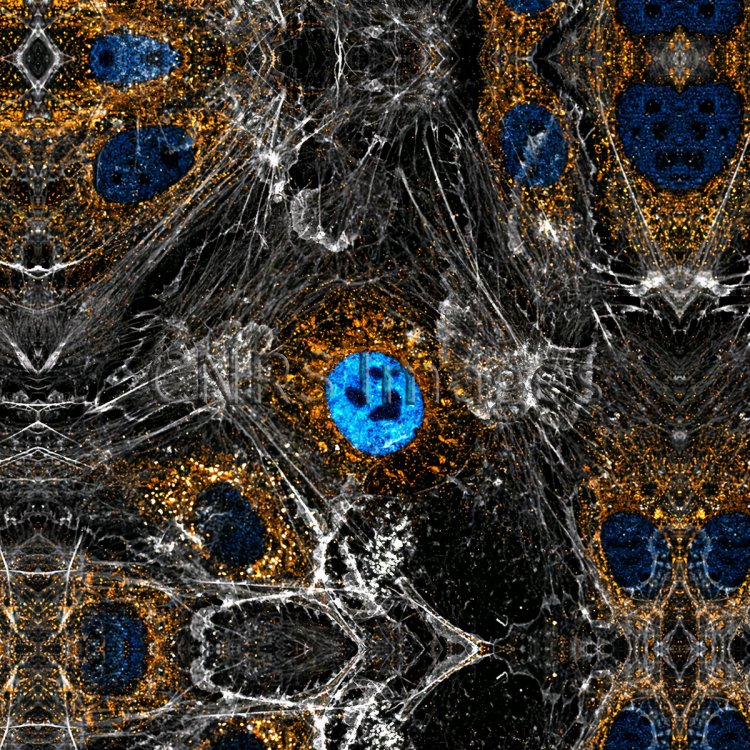
Cette image montre des protéines, en bleu, qui sont soupçonnées d’agir comme messager entre les cellules des vaisseaux sanguins en blanc et leur support moléculaire, en orange. Lors d’un cancer, c’est le système entier qui dysfonctionne.
Les cellules sont entourées d’une matrice qui affecte leur comportement
Contrairement à ce que l’on pourrait penser, les organes et tissus de notre corps ne sont pas composés uniquement de cellules mais plutôt d’un ensemble de cellules variées entourées d’une colle biologique nommée « matrice extracellulaire » qui occupe parfois plus de la moitié du volume d’un tissu. Ce réseau soutient physiquement les cellules, mais il contient aussi des informations mécaniques et chimiques qui contrôlent leur comportement.
Ainsi, certaines protéines de la matrice vont avoir pour effet de favoriser la croissance, la migration cellulaire ou la différenciation des cellules en cellules spécialisées, et même d’influer sur la mort des cellules.
La modification du comportement des cellules en fonction des informations apportées par la matrice extracellulaire s’accompagne, en retour, de la production par les cellules de nouveaux composés de cette matrice contribuant ainsi à son remodelage et à l’adaptation constante des cellules au micro-environnement.
Cet échange permanent d’informations entre les cellules et leur matrice extracellulaire est à la base de ce que l’on appelle l’« homéostasie tissulaire ».
Matrice extracellulaire, cellules et cancers : un grand malentendu !
Au cours du développement des tumeurs, les cellules cancéreuses modifient profondément la composition et l’architecture de la matrice extracellulaire en incitant les autres cellules du tissu à produire des composants qui changent la nature du micro-environnement et le rendre propice à la croissance de la tumeur.
Ce mécanisme, appelé « reprogrammation stromale », est caractérisé par l’expression et la production de protéines matricielles dites « oncofœtales » au sein de la matrice extracellulaire tumorale.
Ces protéines sont normalement présentes essentiellement lors du développement embryonnaire. Lors d’un cancer, elles se trouvent « exprimées » (c’est-à-dire produites) de façon aberrante, et ont pour effet de favoriser la multiplication et la croissance des cellules tumorales. De plus, certaines de ces protéines oncofœtales influencent le comportement des autres cellules présentes dans le tissu en induisant des réponses cellulaires en faveur de la tumeur.
C’est notamment le cas de la fibronectine oncofœtale, en orange sur l’image, qui est produite par les cellules endothéliales (qui tapissent les vaisseaux sanguins) et dont on voit ici le cytosquelette en blanc.
La fibronectine oncofœtale est en grande partie impliquée dans l’« angiogenèse », le mécanisme de formation des nouveaux vaisseaux sanguins à partir de l’arbre vasculaire existant. Alors que la fibronectine oncofœtale est normalement produite par les cellules endothéliales exclusivement lors du développement embryonnaire, sa production peut être réactivée en réponse à la modification du micro-environnement tumoral. Elle favorise alors la survie et la migration des cellules endothéliales lors de l’angiogenèse, et les nouveaux vaisseaux « corrompus » par la tumeur vont alors participer à la croissance tumorale en fournissant des nutriments et de l’oxygène.
De plus, dans les stades avancés des cancers, la création de nouveaux vaisseaux sanguins sous l’influence de l’environnement tumoral permet aux cellules cancéreuses de se disséminer en traversant la couche de cellules endothéliales pour se retrouver dans la circulation sanguine prête à coloniser d’autres organes : c’est le début des métastases.
Comment les cellules endothéliales interprètent-elles les signaux de la tumeur ?
Comprendre comment les cellules des vaisseaux sanguins interprètent les signaux de la tumeur est une question majeure de la recherche fondamentale en cancérologie.
En effet, réussir à décrypter comment ces messages sont transmis à l’intérieur des cellules endothéliales pourrait permettre de « bloquer » les communications entre la matrice extracellulaire tumorale et les cellules endothéliales, voire de stopper la production locale de matrice extracellulaire par les cellules endothéliales, et donc d’empêcher leur survie et leur migration vers la tumeur.
À ce jour, il y a eu plusieurs tentatives infructueuses de blocage de l’angiogenèse (en utilisant des antagonistes des récepteurs de la matrice extracellulaire présents à la surface des cellules endothéliales), d’où l’importance d’essayer de mieux comprendre les bases du dialogue entre les cellules et la matrice.
Parmi les nouveaux candidats impliqués dans la transmission des messages « pro-tumoraux » de la matrice extracellulaire tumorale vers les cellules endothéliales se trouvent les protéines liant les ARN. Nous étudions plus particulièrement le rôle de la protéine SAM68 (article en préparation), que l’on voit ici en bleu dans les noyaux des cellules endothéliales. Nos résultats préliminaires montrent que SAM68 participe à la transformation des signaux extracellulaires en messages moléculaires dans les cellules. Ces messages vont conduire à une production de nouveaux composés de la matrice extracellulaire, comme la fibronectine oncofœtale.

Article publié initialement dans The Conversation.
Science infuse est un service de presse en ligne agréé (n° 0324 x 94873) piloté par Citizen4Science, association à but non lucratif d’information et de médiation scientifique doté d’une Rédaction avec journalistes professionnels. Nous défendons farouchement notre indépendance. Nous existons grâce à vous, lecteurs. Pour nous soutenir, faites un don ponctuel ou mensuel.
ou via J’aime l’Info, partenaire de la presse en ligne indépendante